前回の記事では、逐次重合における反応率 $p$ と数平均重合度 $\overline{X_n}$ の関係を示す「カロザースの式」の基本形($\overline{X_n} = \frac{1}{1 – p}$)をゼロから導出しました。
前回の記事をご覧になる方はこちらからご確認ください。
しかし、この基本式には「2つの成分(A成分とB成分)が完全に同じ数(等モル)存在する」という理想的な大前提があります。現実の実験や工場では、どんなに精密な天秤を使っても、一滴の狂いもなく完全に1:1で量り取ることは不可能です。
今回は、このようにモル比がずれた場合(非化学量論的)にカロザースの式がどう変化するのか、その導出(証明)を行い、なぜ高分子の合成では「等モル」に近づけることが極めて重要なのかを解説します!
新しい主役「モル比 r」の導入
まずは、A成分(例:ジカルボン酸)とB成分(例:ジアミン)が混ざっている状態を定義します。
- $N_a$ : A成分の分子の数
- $N_b$ : B成分の分子の数
ここで、数が少ない方をA成分と定義します(つまり $N_a \le N_b$ )。
このとき、モル比 $r$ を次のように定義します。
$$r = \frac{N_a}{N_b}$$
- AとBが完全に同じ数(等モル)のとき: $r = 1$
- Bの方が少し多いとき: $r < 1$ (例:Aが99個、Bが100個なら $r = 0.99$)
このように、$r$ は常に $r \le 1$ となる数値です。
拡張版カロザースの式の導出(証明)
それでは、モル比 $r$ が組み込まれた「拡張版カロザースの式」を、前回の導出と同じように「分子の数を数える」というアプローチで証明していきましょう。
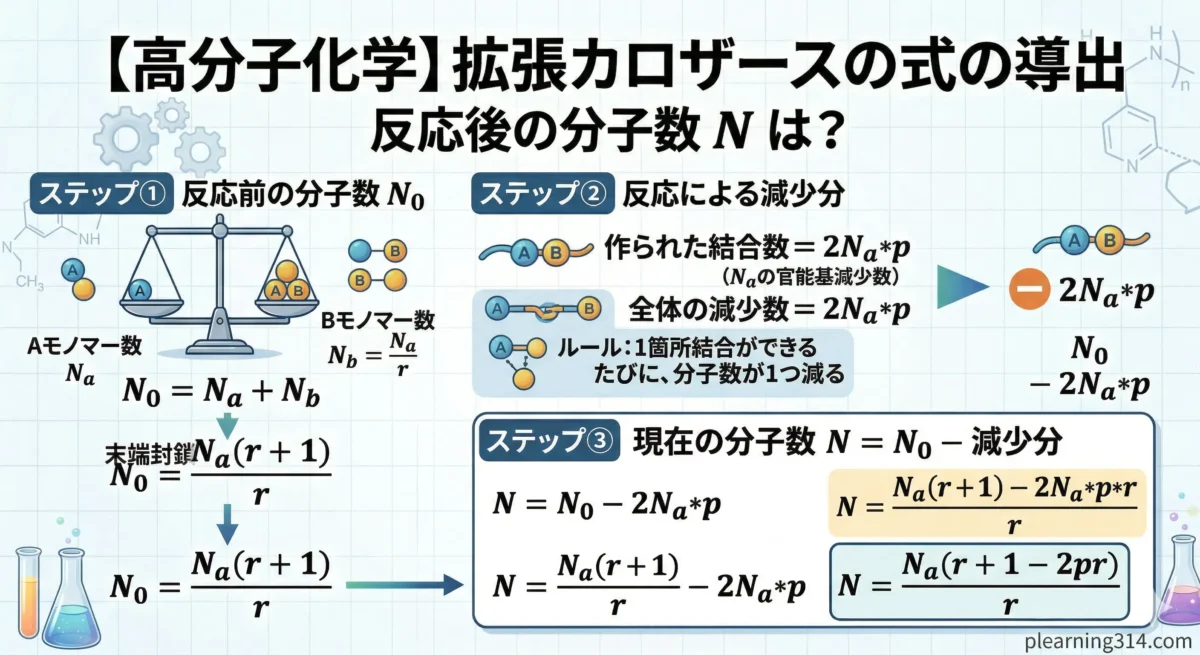
ステップ①:最初の分子の総数 $N_0$ を求める
反応前のバラバラなモノマーの総数 $N_0$ は、A成分とB成分の合計です。
$$N_0 = N_a + N_b$$
これを、$N_a$ と $r$ だけを使った式に変形します。定義より $N_b = \frac{N_a}{r}$ なので、これを代入します。
$$N_0 = N_a + \frac{N_a}{r} = N_a \left(1 + \frac{1}{r}\right) = \frac{N_a (r + 1)}{r}$$
ステップ②:反応後の分子の総数 $N$ を求める
次に、反応率 $p$ まで反応が進んだときの、全体の分子数 $N$ を考えます。
ここでいう反応率 $p$ は、「数が少ない方のA成分の官能基が、どれくらい反応したか」を表します。
A成分の分子1個には官能基(手)が2つあるので、Aの官能基の総数は $2N_a$ 個です。
反応率が $p$ のとき、実際に手を繋いだ(反応した)Aの官能基の数は $2N_a p$ 個 になります。
逐次重合では「1箇所結合ができる(手が繋がる)たびに、全体の分子の数が1つ減る」というルールがありましたね。
つまり、作られた結合の数($= 2N_a p$)だけ、最初の分子数 $N_0$ から引き算すれば、現在の分子数 $N$ が出ます。
$$N = N_0 – 2N_a p$$
ここに、ステップ①で求めた $N_0 = \frac{N_a(r + 1)}{r}$ を代入して整理します。
$$N = \frac{N_a (r + 1)}{r} – 2N_a p$$
$$N = \frac{N_a (r + 1) – 2N_a p r}{r} = \frac{N_a (r + 1 – 2pr)}{r}$$
ステップ③:数平均重合度 $\overline{X_n}$ の定義式に代入する
数平均重合度の定義は「最初の分子数 $\div$ 現在の分子数」でしたね。
$$\overline{X_n} = \frac{N_0}{N}$$
ここに、ステップ①と②で求めた式を代入します!
$$\overline{X_n} = \frac{\frac{N_a(r + 1)}{r}}{\frac{N_a(r + 1 – 2pr)}{r}}$$
分母と分子にある $N_a$ と $r$ が綺麗に約分されて消えます。
$$\overline{X_n} = \frac{1 + r}{1 + r – 2rp}$$
これで拡張版カロザースの式の証明は完了です!
(※もし完全に等モル($r = 1$)だった場合、この式に $r = 1$ を代入すると $\frac{2}{2 – 2p} = \frac{1}{1 – p}$ となり、基本の式にちゃんと戻ることが確認できます)
なぜ「等モル」がそれほど重要なのか?
証明できたこの式を使って、実験で「等モル」にすることがどれほど重要なのかを計算してみましょう。
「反応を極限まで(100%)進めた場合」を考えてみます。式に反応率 $p = 1$ を代入します。
$$\overline{X_n} = \frac{1 + r}{1 + r – 2r} = \frac{1 + r}{1 – r}$$
この $\overline{X_n} = \frac{1 + r}{1 – r}$ という式は、「モル比が $r$ のとき、どれだけ頑張って反応させても、これ以上は絶対に分子が長くならない限界の重合度」を表しています。
わずかな量り間違いが命取りに
もし、量り間違えによってモル比が少しだけずれてしまった場合、限界の重合度はどうなるでしょうか?
- ズレなし($r = 1.000$)の場合分母が $0$ になるため、$\overline{X_n}$ は無限大($\infty$)になります。理論上はどこまでも巨大な高分子に成長できます。
- たった1%ズレた($r = 0.990$)の場合$$\overline{X_n} = \frac{1 + 0.99}{1 – 0.99} = \frac{1.99}{0.01} = 199$$反応率を100%にしても、重合度はたったの 199 でストップしてしまいます。
- 5%ズレた($r = 0.950$)の場合$$\overline{X_n} = \frac{1 + 0.95}{1 – 0.95} = \frac{1.95}{0.05} = 39$$重合度は 39 で止まります。この重合度で高分子と呼ぶことはできません。また、これではプラスチックとしての強度は全く出ず、ボロボロの粉やドロドロの液体になってしまいます。
なぜ成長が止まるのか?(直感的なイメージ)
B成分が少し多い状態($r < 1$)で反応を進めると、最終的にすべての鎖の両端が、余っている「B成分の官能基」になってしまいます。
「Bの端っこ」同士は反応できないため、そこで鎖の成長が完全にストップしてしまうのです。(これを末端封鎖と呼びます)
だからこそ、逐次重合で強度の高い立派なプラスチックを作るためには、「極限まで反応率 $p$ を高める」ことと同時に、「極限までモル比 $r$ を 1 に近づける(等モルにする)」という2つの厳しい条件をクリアしなければならないのです。
逆転の発想:あえてズラす「分子量制御」
「モル比がずれると分子量が上がらない」というのは一見するとデメリットですが、工場などではこの性質をあえて利用することがあります。
例えば、「重合度をちょうど100ぐらいにコントロールして、加工しやすいサラサラの樹脂を作りたい」という場合です。等モルで反応させると、反応が進みすぎてドロドロになりすぎる危険があります。
そこで、あえて最初に $r = 0.98$ 程度になるように原料を混ぜておきます。そうすれば、どれだけ反応が進んでも「重合度99」付近で自動的に反応が止まり、常に一定の品質のポリマーを安定して作ることができるのです。
まとめ
- 実際の重合では、モル比 $r = \frac{N_a}{N_b}$ を考慮した拡張式 $\overline{X_n} = \frac{1 + r}{1 + r – 2rp}$ が使われる。
- 導出は「最初の分子数」から「反応した官能基の数(=減った分子の数)」を引くだけ。
- 反応率を100%($p=1$)にしても、モル比がずれていると末端が封鎖され、重合度は $\frac{1+r}{1-r}$ でストップしてしまう。
- この性質を逆手にとることで、目標の分子量にピタリと制御することができる。
数式アレルギーになりそうな分野ですが、一つひとつの記号の意味と「鎖の末端」をイメージできれば、高分子化学の面白さがグッと増してくるはずです!
コメント