高分子材料を扱う上で、「このプラスチックは何℃まで耐えられるのか?」「結晶化しているのか?」を知ることは非常に重要です。これらを一発で測定できるのがDSC(Differential Scanning Calorimetry:示差走査熱量計)です。
今回は、高分子の「体温計」とも言えるDSCについて解説します。
DSCとは?
DSCは、サンプル(試料)とリファレンス(基準物質)の温度を一定のスピードで上げていき、その過程で発生する「熱の出入り(吸熱・発熱)」を測定する装置です。
- 吸熱反応: 氷が溶ける時のように、周囲から熱を奪う反応。
- 発熱反応: 固まる時や反応する時のように、周囲に熱を放出する反応。
これを見ることで、目には見えないミクロな分子の状態変化が手に取るように分かります。
測定原理:温度の「足並み」をそろえる
DSCの装置の中には、小さなアルミパンが2つ並んでいます。
- サンプル: 測りたいプラスチックの破片など。
- リファレンス: 中身が空のアルミパン。
装置は、この2つの温度が常に同じになるように加熱します。しかし、途中でサンプルが「溶ける(融解)」などの変化を起こすと、そこだけ余計にエネルギー(熱量)が必要になります。この「リファレンスに対してどれだけ余計に(あるいは少なく)熱を加えたか」を記録するのがDSCの仕組みです。
DSC曲線の読み方:4つの重要ポイント
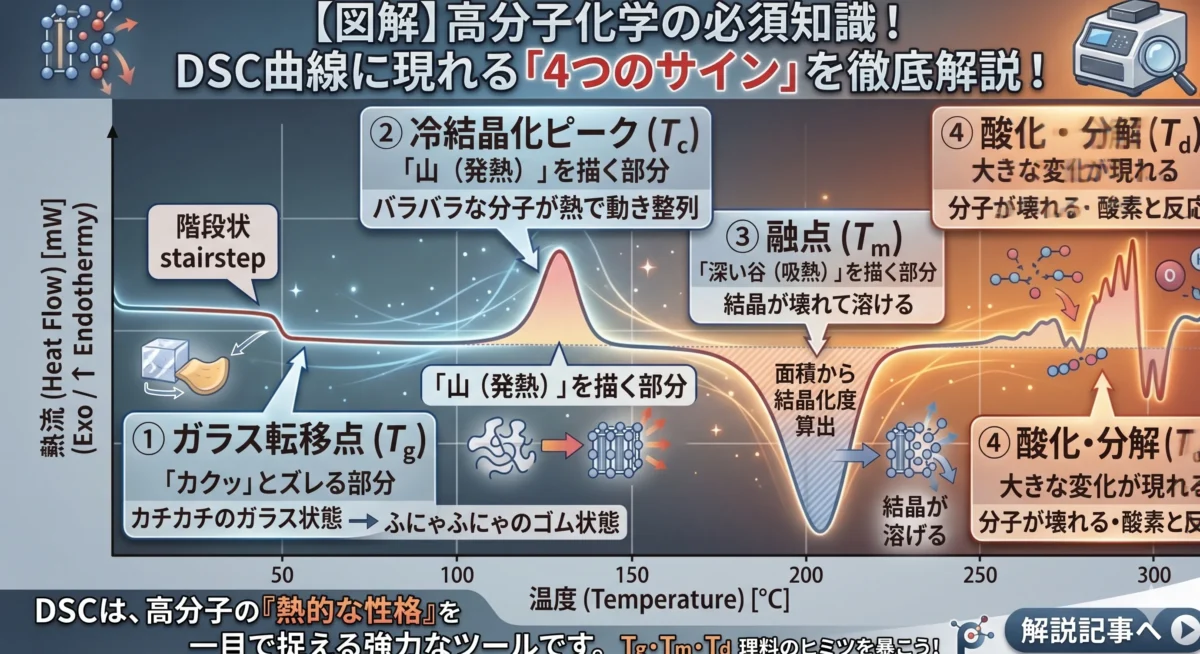
DSCのグラフ(DSC曲線)には、高分子の性格を表す独特なサインが現れます。
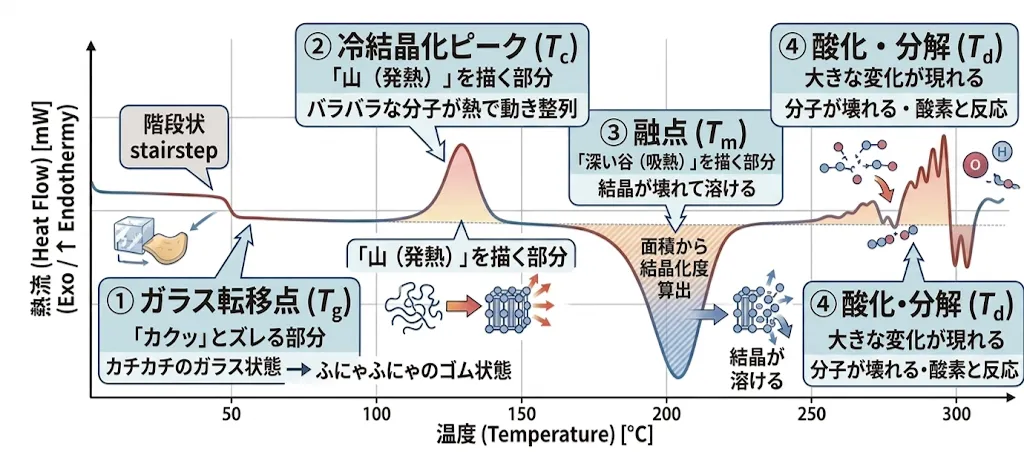
① ガラス転移点($T_g$)
グラフが階段状に「カクッ」とズレる部分です。
高分子が「カチカチのガラス状態」から「ふにゃふにゃのゴム状態」に変わる温度です。この温度を超えると、材料の強度がガクンと落ちるため、耐熱性を判断する上で最も重要な指標の一つです。
② 冷結晶化ピーク($T_c$)
グラフが「山(発熱)」を描く部分です。
バラバラだった分子鎖が、熱を得て動きやすくなり、綺麗に整列して「結晶」を作る時に熱を放出します。
③ 融点($T_m$)
グラフが「深い谷(吸熱)」を描く部分です。
結晶がバラバラに壊れてドロドロに溶ける際、大量の熱を吸収します。このピークの面積を測ることで、そのプラスチックがどれくらい「結晶化」しているか(結晶化度)を計算できます。
④ 酸化・分解($T_d$)
さらに温度を上げると、分子が壊れたり酸素と反応したりして、大きな変化が現れます。
DSCで何がわかる?(実務での活用例)
研究や品質管理の現場では、以下のような目的で使われます。
- 材料の特定: 融点が160℃ならポリプロピレン(PP)、260℃ならナイロン66、といった具合に「指紋」のように使えます。
- リサイクル材の混入確認: 本来ないはずの温度に小さなピークがあれば、「別のプラスチックが混ざっているな」と見抜けます。
- 成形条件の最適化: 「何度で冷やせば一番きれいに固まるか」をシミュレーションできます。
まとめ
DSCは、温度変化に対する分子の「悲鳴(吸熱)」や「歓喜(発熱)」を可視化するツールです。
FT-IRで成分を知り、GPCで大きさを知り、DSCで熱の性質を知る。この3つが揃えば、高分子分析はマスターしたも同然です!
コメント