ここでは化学や物理の分野で一般的に用いられる絶対温度と呼ばれる温度と気体・液体・固体の物質の三態について解説していきます.
絶対温度
温度を表す単位にはいくつか種類があります.日常生活で一般的に用いられているのは℃という単位です.これはセルシウス温度と呼ばれます.このセルシウス温度は水の融点を0℃,水の沸点を100℃として定義されます.
化学の分野ではこのセルシウス温度も使われますが,絶対温度という温度の方が頻繁に用いられます.この絶対温度の単位はケルビンKであり,ケルビン温度と呼ばれることもあります.絶対温度での0Kとは分子の運動が完全に停止しするような温度です.この0Kは絶対零度と呼ばれます.
そもそも分子の運動とは何でしょうか.0Kよりも大きな温度では物質は全て動き回っています.この動きのことを運動と呼びます.気体の場合はこの運動が顕著であり,自由に飛び回っています.液体の場合は気体よりは運動が制限されますが,自由に動き回っています.固体になるとさらに運動が制限されあまり動くことはできません.しかし,若干振動するなどして運動をしています.0Kではこのわずかな振動すらも起こらなくなり,完全に運動が停止してしまうのです.
セルシウス温度と絶対温度では1℃の間隔が同じです.ですので1Kの差は1℃の差と同じになります.絶対温度とセルシウス温度には次の式の関係が成り立ちます.
[K]=[℃]+273.15
つまり,0℃では273.15Kということになります.また絶対零度0Kは-273.15℃になります.絶対温度とセルシウス温度はこの式で変換できます.
物質の三態
物質には固体,液体,気体という3つの状態があります.このそれぞれの状態の変化には名前がついています.固体から液体への変化を融解,液体から固体への変化を凝固,液体から気体への変化を蒸発,気体から液体への変化を凝縮,固体から気体および気体から液体への変化をどちらも昇華と呼びます.これを図にすると次のようになります.
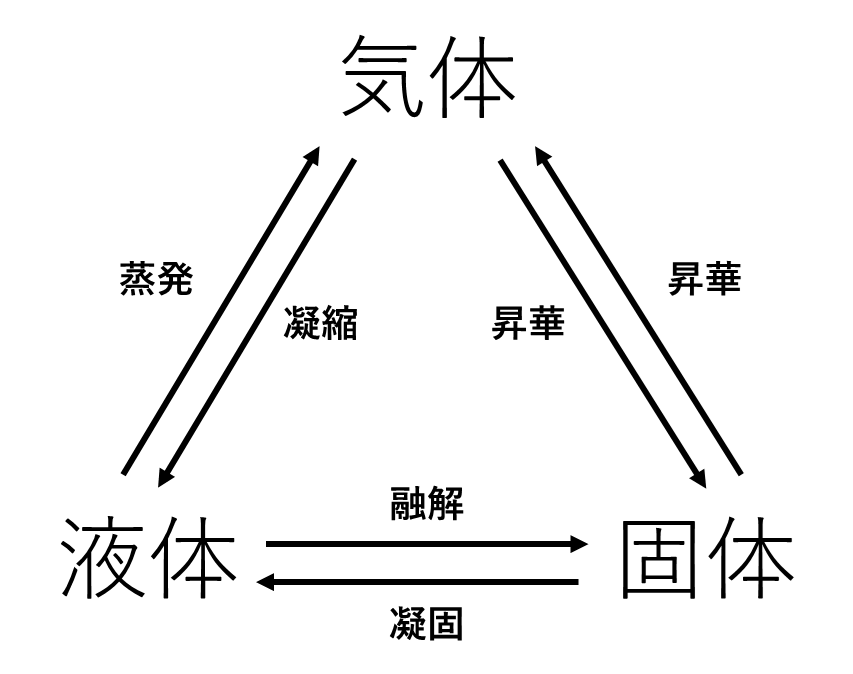
固体から気体に変化する昇華はあまりイメージがつかないかもしれませんが,有名なものだとドライアイスがあります.ドライアイスは固体の状態から液体にならずに気体の二酸化炭素になります.
また,融解する温度を融点,凝固する温度を凝固点,沸騰する温度を沸点と呼びます.ここで,融点と凝固点は同じ温度になります.
純粋な物質(他に何も混ざっていない物質)の場合,固体,液体,気体という状態は温度と圧力により決まります.ある温度,圧力のときにどの状態をとるかを表した図を状態図と呼びます.下に水の状態図を示します.
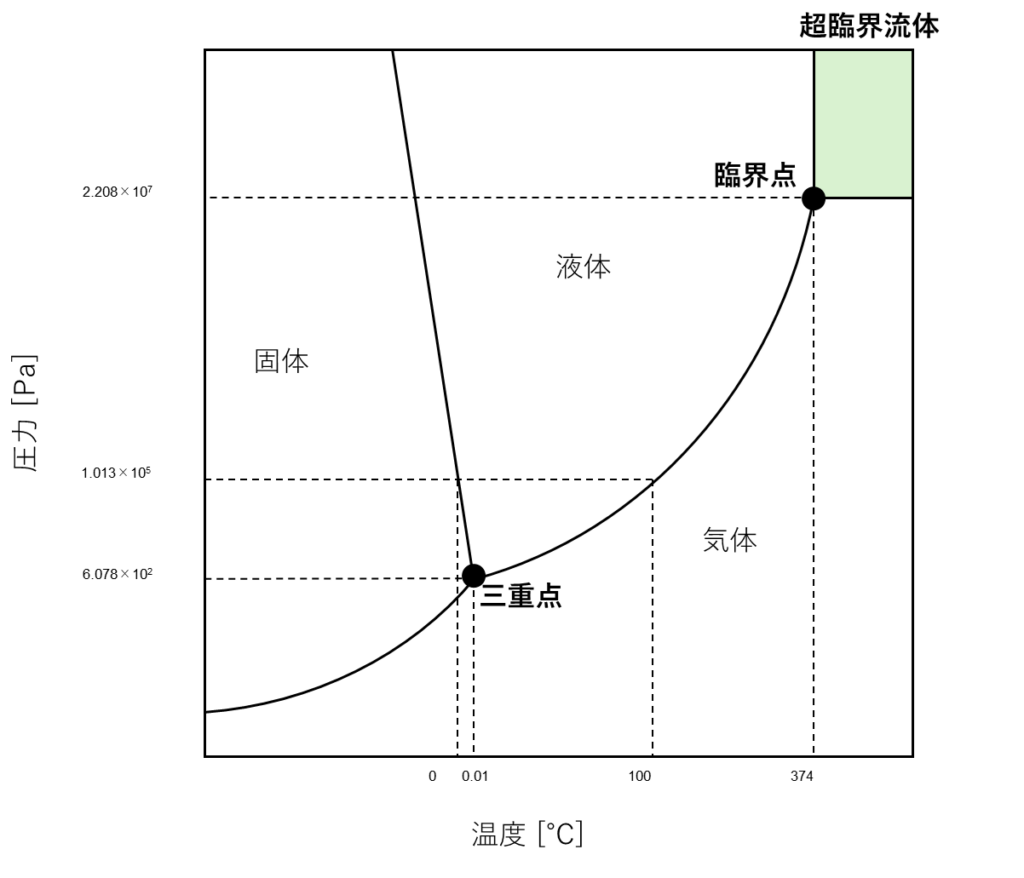
縦軸が圧力,横軸が温度を表しています.右上の黄緑色の部分を除くと,曲線で3つの部分に分かれています.曲線で分けられた3つの領域の中にあるとき,図に書いてある状態をとります.大気圧と同じ1.013×105Paの点線をたどって見てみましょう.この点線上では低温側ではまず固体の領域にあります.ここから右に進むと曲線にあたります.ここでの温度は0℃であり,この温度よりも高くなると液体になります.つまり,この曲線を右から左に横切ることが融解に当たるのです.さらに右に進むと再び曲線と出くわし,それを超えると気体になります.この曲線と交わった点における温度は100℃になり,この点が沸点になります.
このように固体と液体を分けている曲線は融解に対応し,液体と気体を分けている曲線は沸騰に対応しています.また,固体と気体を分けている曲線は昇華に対応します.そのため,固体と液体を分けている曲線を融解曲線,液体と気体を分けている曲線を蒸気圧曲線,固体と気体を分けている曲線を昇華曲線と呼びます.さらに,これら3つの曲線が交わっている点は固体と液体と気体の3つが共存した状態になります.ですのでこの点のことを三重点と呼びます.
また,状態図の右上を見ると緑色で囲われている部分があります.この部分では液体とも気体とも区別がつかない特別な状態となります.そのため,この状態のことを超臨界状態と呼び,超臨界状態の物質を超臨界流体といいます.そして,この超臨界状態に切り替わる温度,圧力の場所を臨界点と呼びます.この超臨界状態は高温,高圧の条件にしない限り出現しないため普通に生活しているときに見ることはできません.これだけでは超臨界状態はかなりわかりにくいと思いますので気になる方はYouTubeの動画をこちらから確認してみてください.
他の物質の状態図も確認してみましょう.二酸化炭素の状態図は下のようになります.
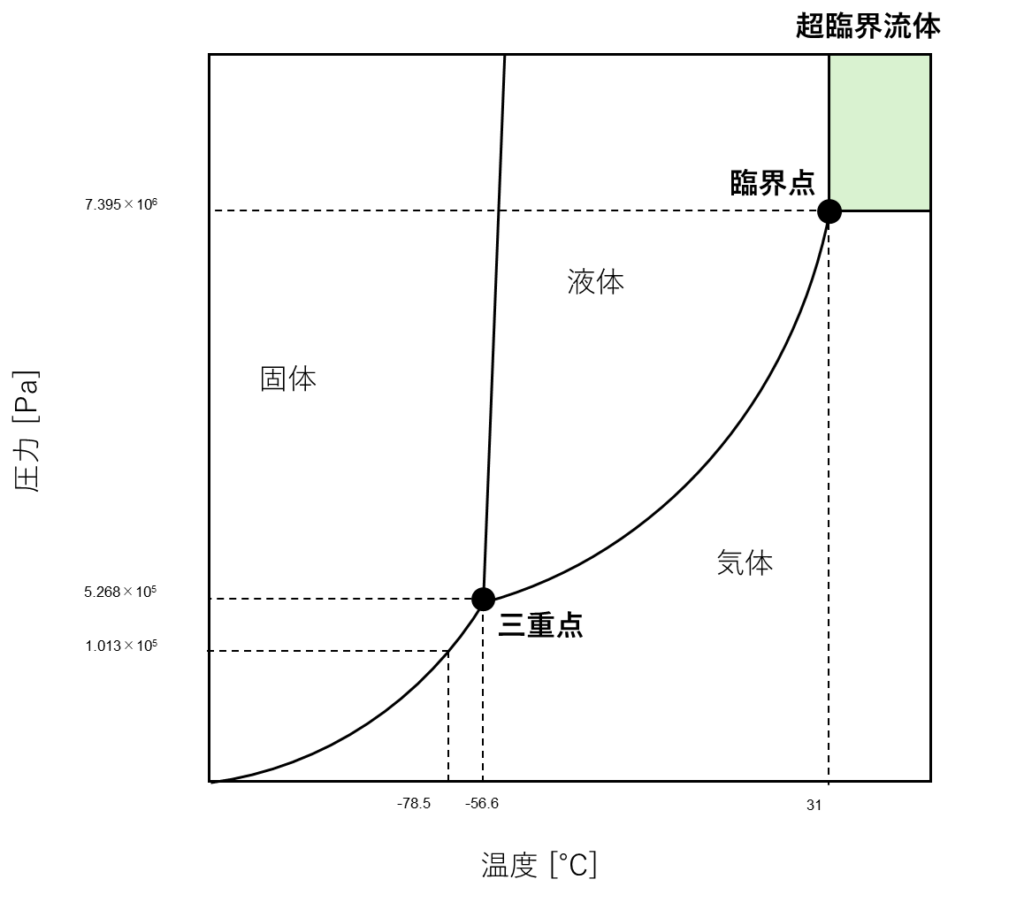
形だけ見ると,二酸化炭素の場合も水と同じになります.基本的に,どの物質であってもかたちは似たものになります.唯一違うのが温度と圧力の大きさです.二酸化炭素の場合,大気圧の1.013×105Paでは低温側からたどっていくと固体の状態から-56.6℃で気体に変化します.図から分かるとおり,大気圧では液体が存在しません.ですので,液体の二酸化炭素を見るには圧力をかけなければなりません.
では,この状態図について少し問題を解いてみましょう.
問題
下の状態図中の①,②,③の矢印の変化は融解,蒸発などのうちなんと呼ばれる変化か説明してください.

解答
①融解(固体から液体への変化)
②蒸発(液体から気体への変化)
③昇華(気体から固体への変化)
まとめ
以上,絶対温度と物質の三態でした.
化学においては℃の他に絶対温度Kが用いられます.℃とKの変換は[K]=[℃]+273.15で計算されます.
また,物質には気体,液体,固体の3つの状態があり,各状態の変化には凝縮,凝固,蒸発,融解,昇華と名前がついています.これらの状態は温度と圧力に依存し,その関係を表した図を状態図と呼びます.高温,高圧状態では超臨界状態と呼ばれる特殊な状態が存在しています.
今回の記事で少しでも理解の一助になりましたら幸いです.ご不明な点がございましたらお気軽にお問い合わせください.



コメント