今回のゴールは、前回の記事で登場した以下のMayo-Lewis式を導き出すことです。
$$\frac{d[M_1]}{d[M_2]} = \frac{[M_1]}{[M_2]} \cdot \frac{r_1[M_1] + [M_2]}{r_2[M_2] + [M_1]}$$
- $[M_1], [M_2]$ :フラスコ内のモノマー濃度(仕込み量)
- $d[M_1]/d[M_2]$ :ポリマーに取り込まれる速度の比(できあがるポリマーの組成)
それでは、4つのステップで導出していきましょう!
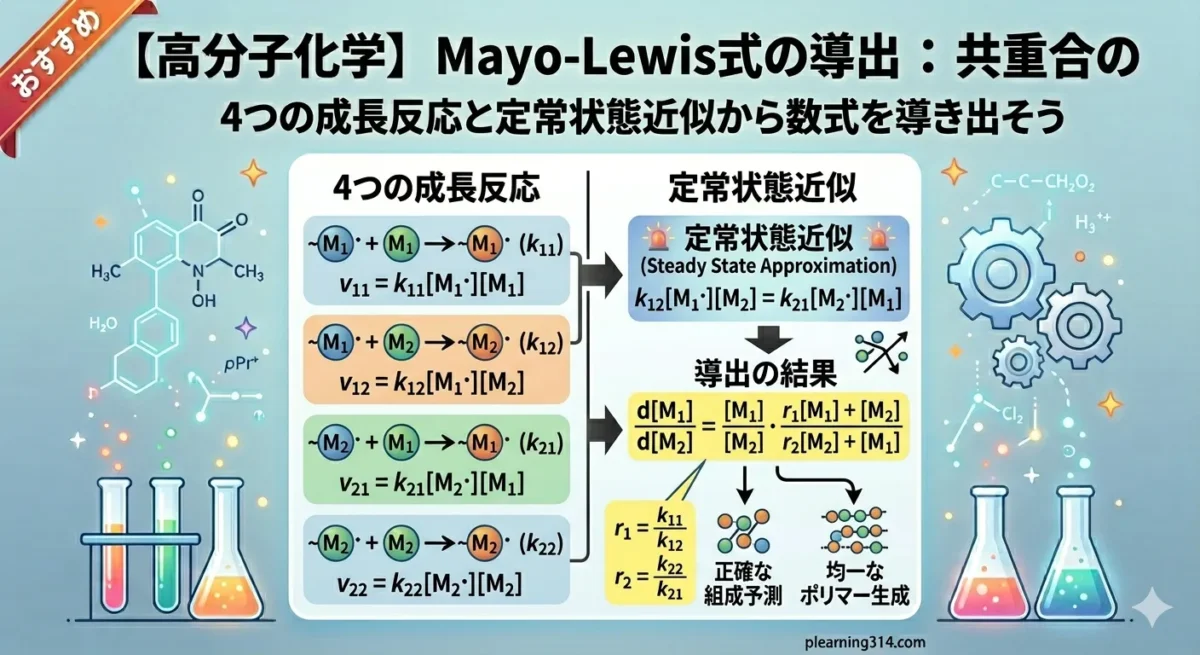
ステップ1:4つの成長反応を書き出す
共重合の反応容器の中では、2種類の成長末端ラジカル($\sim M_1\cdot$ と $\sim M_2\cdot$)と、2種類のモノマー($M_1$ と $M_2$)が入り乱れています。
この組み合わせにより、ポリマーが成長するパターンは以下の4つしかありません。
- $M_1$末端が $M_1$を食べる(速度定数 $k_{11}$)
$\sim M_1\cdot + M_1 \xrightarrow{k_{11}} \sim M_1\cdot$
反応速度:$v_{11} = k_{11}[M_1\cdot][M_1]$ - $M_1$末端が $M_2$を食べる(速度定数 $k_{12}$)
$\sim M_1\cdot + M_2 \xrightarrow{k_{12}} \sim M_2\cdot$
反応速度:$v_{12} = k_{12}[M_1\cdot][M_2]$ - $M_2$末端が $M_1$を食べる(速度定数 $k_{21}$)
$\sim M_2\cdot + M_1 \xrightarrow{k_{21}} \sim M_1\cdot$
反応速度:$v_{21} = k_{21}[M_2\cdot][M_1]$ - $M_2$末端が $M_2$を食べる(速度定数 $k_{22}$)
$\sim M_2\cdot + M_2 \xrightarrow{k_{22}} \sim M_2\cdot$
反応速度:$v_{22} = k_{22}[M_2\cdot][M_2]$
ステップ2:モノマーの消費速度の式を立てる
次に、「$M_1$と$M_2$が、それぞれどれくらいのスピードで減っていくか(=ポリマーに取り込まれるか)」を式にします。
$M_1$が消費されるのは、上記のパターンのうち「1」と「3」のときです。
$$-\frac{d[M_1]}{dt} = k_{11}[M_1\cdot][M_1] + k_{21}[M_2\cdot][M_1]$$
消費される速さなので「$-$」がついています。
同じように、$M_2$が消費されるのは「2」と「4」のときです。
$$-\frac{d[M_2]}{dt} = k_{12}[M_1\cdot][M_2] + k_{22}[M_2\cdot][M_2]$$
知りたいのは「$M_1$と$M_2$がポリマーに入る割合(比率)」なので、上の式を下の式で割り算します。時間 $dt$ とマイナス符号が消えて、以下の式になります。
$$\frac{d[M_1]}{d[M_2]} = \frac{k_{11}[M_1\cdot][M_1] + k_{21}[M_2\cdot][M_1]}{k_{12}[M_1\cdot][M_2] + k_{22}[M_2\cdot][M_2]} \quad \cdots \text{(A)}$$
ステップ3:魔法の前提条件「定常状態近似」
式(A)には、私たちが測定できない「ラジカル濃度($[M_1\cdot], [M_2\cdot]$)」が含まれていて、このままでは計算できません。ここで、高分子化学における超重要テクニック「定常状態近似(Steady-State Approximation)」を使います。
ラジカルは非常に不安定なので、「$M_1\cdot$ から $M_2\cdot$ に変わるスピード」と、「$M_2\cdot$ から $M_1\cdot$ に戻るスピード」は、常に釣り合って一定になっていると仮定します。
- $M_1\cdot \rightarrow M_2\cdot$ になる反応(ステップ1の「2」): $k_{12}[M_1\cdot][M_2]$
- $M_2\cdot \rightarrow M_1\cdot$ になる反応(ステップ1の「3」): $k_{21}[M_2\cdot][M_1]$
これが釣り合っているので、以下の等式が成り立ちます!
$$k_{12}[M_1\cdot][M_2] = k_{21}[M_2\cdot][M_1] \quad \cdots \text{(B)}$$
ステップ4:代入して整理する(ゴール!)
あとは、この式(B)を使って式(A)から邪魔なラジカル濃度を消し去るだけです。
式(A)の分子と分母を、式(B)の両辺(同じ値なので割ってもOK)でそれぞれ割ってみましょう。
【分子を $k_{21}[M_2\cdot][M_1]$ で割る】
$$\frac{k_{11}[M_1\cdot][M_1]}{k_{21}[M_2\cdot][M_1]} + 1$$
ここで、分母の $k_{21}[M_2\cdot][M_1]$ を 式(B)より $k_{12}[M_1\cdot][M_2]$ に置き換えると…
$$\frac{k_{11}[M_1\cdot][M_1]}{k_{12}[M_1\cdot][M_2]} + 1 = \frac{k_{11}}{k_{12}} \cdot \frac{[M_1]}{[M_2]} + 1$$
【分母を $k_{12}[M_1\cdot][M_2]$ で割る】
$$1 + \frac{k_{22}[M_2\cdot][M_2]}{k_{12}[M_1\cdot][M_2]}$$
同じように、分母の $k_{12}[M_1\cdot][M_2]$ を $k_{21}[M_2\cdot][M_1]$ に置き換えると…
$$1 + \frac{k_{22}[M_2\cdot][M_2]}{k_{21}[M_2\cdot][M_1]} = 1 + \frac{k_{22}}{k_{21}} \cdot \frac{[M_2]}{[M_1]}$$
ここで、前回の記事で定義した「モノマー反応性比」を思い出してください。
$r_1 = k_{11}/k_{12}$ 、 $r_2 = k_{22}/k_{21}$ でしたね!これを当てはめると、式(A)は次のように進化します。
$$\frac{d[M_1]}{d[M_2]} = \frac{r_1 \frac{[M_1]}{[M_2]} + 1}{1 + r_2 \frac{[M_2]}{[M_1]}}$$
最後に、この分数の形を見やすくするために、分母と分子を「通分」して整理します。
分子は $\frac{r_1[M_1] + [M_2]}{[M_2]}$ 、分母は $\frac{[M_1] + r_2[M_2]}{[M_1]}$ となるので……
$$\frac{d[M_1]}{d[M_2]} = \frac{[M_1]}{[M_2]} \cdot \frac{r_1[M_1] + [M_2]}{r_2[M_2] + [M_1]}$$
証明完了です!!!
(おまけ)モル分率 $f, F$ の式への変換
グラフを描くときによく使う「モル分率(割合)」の式にするには、ここから少しだけ変形します。
- 仕込みモル分率の比: $\frac{[M_1]}{[M_2]} = \frac{f_1}{f_2}$
- ポリマー組成のモル分率の比: $\frac{d[M_1]}{d[M_2]} = \frac{F_1}{F_2}$
これを代入し、$F_1 + F_2 = 1$、$f_1 + f_2 = 1$ という関係を使って $F_1 = \cdots$ の形に解き直すと、よく見るあの最終形態になります。
$$F_1 = \frac{r_1 f_1^2 + f_1 f_2}{r_1 f_1^2 + 2f_1 f_2 + r_2 f_2^2}$$
まとめ
一見すると呪文のようなMayo-Lewis式も、分解してみれば「4つの反応パターン」と「定常状態近似」という当たり前の物理現象を数式に翻訳しただけであることがわかります。
「消費速度を割り算して、定常状態近似でラジカルを消す!」という流れだけ思い出せば、必ず最後まで辿り着けますよ!

コメント